|
Procedure |
Extraction |
Proposed fraction |
Advantages |
Shortcomings |
SMT
(Ruban et al.,
2001) |
a. NaOH 1 M (extract+3.5 M HCl)
b. 1 M HCl
c. HCl 1 M
d. HCl 1 M +calcination
e. HCl 3.5 M +calcination |
NaOH-P
HCl-P
IP
OP
Conc. HCl-P |
Simple, practical |
partial resorption of P extracted by NaOH on CaCO3 |
Jensen
(1998) |
a. MgCl2
1 M
b. DB 0.11 M
c. NaOH 0.1 M
d. Acetate buffer 1M
e. HCl 0.5 M
f. ignition+HCl 1 M boilling |
loosely adsorbed IP and leachable OP
iron-bound IP
adsorbed IP and leachable OP
authigenic apatite, CaCO3-bound
IP and leachable OP
detrital apatite
refractory OP |
separating authigenic
CFAP from detrital FAP |
very long;
not practical;
resorption by carbonates in calcareous sediments |
Golterman
(1996) |
a. H2O
b. Ca-EDTA 0.05 M + dithionite
c. Na2-EDTA 0.1 M
e. H2SO4 0.25 M
f. NaOH 2 M |
labile P bioavailable
iron-P bioavailable
Ca-P non-available
acid soluble organic P bioavailable
reductant Organic P non-available |
giving more information on the quantity of P available
for algae |
not practical;
EDTA interfere with P determination;
complicated solution preparation;
in some sediments, extraction must be repeated |
Penn
(1995) |
a. NH4Cl
1 M (3×)
b. NaOH 0.1 M (split)
c. NaOH 0.1 M (split)
d. HCl 0.5 M
e. Persulfate digestion |
loosely bound-P
loosely sorbed and CaCO3 associated-P
Fe and Al bound-P
extractable biogenic-P
calcium mineral-P
refractory organic-P |
dissolution of small
amounts of Fe-P and
Al-P by NH4Cl was
avoided |
hydrolysis of organic P;
no relation with bioavailability |
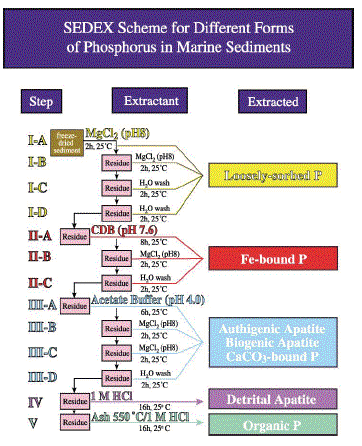
SEDEX
(Ruttenberg,
1992) |
a. MgCl2
1 M
b. CDB 0.3/1 M
c. Acetate buffer 1 M
e. HCl 1 M
f. calcination+HCl 1M |
loosely sorbed P
ferric Fe-bound P
CFAP+ biogenic apatite+CaCO3-P
detrital apatite
organic P |
separating authigenic
CFAP from detrital FAP |
very long;
not practical;
partial OP released by CD |
Williams
(Burrus et al.,
1990) |
a. NaOH 1 M
b. HCl 1+3.5 M
c. HCl 3.5 M+calcination
d. HCl 1 M +calcination |
non-apatite P
apatite P
total P
organic P |
Simple, practical |
partial resorption of P extracted by NaOH on CaCO3 |
Psenner
(1988) |
a. NH4Cl
1 M
b. DB 0.11 M 40 ℃
c. NaOH 1 M
d. NaOH 1M
e. HCl 0.5 M |
soluble P
reductant-soluble P
Fe- and Al-bound P
refractory OP
Ca-bound P |
identifying discrete P
compounds |
resorption by carbonates in
calcareous sediments;
hydrolysis of organic P |
Hieltjes and Lijklema
(1980) |
a. NH4Cl
1 M pH 7
b. NaOH 0.1 M
c. HCl 0.5 M |
labile P
Fe- and Al-bound P
Ca-bound P |
Simple, practical |
dissolution of small amounts of Fe-P and Al-P by
NH4Cl; hydrolysis of
organic P;
no relation with bioavailability |
Williams
(1976) |
a. CDB 0.22/0.1 M
b. NaOH 1 M
c. HCl 0.5 M |
non-apatite P
apatite P
organic P |
Simple, practical |
resorption by carbonates in
calcareous sediments
Ca-P and org-P released by CDB |
Chang and Jackson
(1957) |
a. NH4Cl
1 M
b. NH4F 0.5 M pH 8.2
c. NaOH 0.1 M
d. HCl 0.5 M
e. CDB
f. NaOH |
labile P
Al-bound P
Fe-bound P
Ca-bound P
reductant-soluble P
refractory P |
identifying discrete P compounds |
extraction of Fe-P by NH4F
resorption by CaF2
precipitation of phosphate with iron |
/Image1870.gif)
/Image1871.gif)
/Image1872.gif)
/Image1873.gif)
/Image1874.gif)
/Image1875.gif)
/Image1866.gif)
/Image1869.gif)
/Image1867.gif)
/Image1868.gif)
/Image1876.gif)